Kısmi basınç sorusu nasıl çözülür?
Gaz karışımlarında her bir bileşenin basınç katkısını anlamak için kısmi basınç kavramı temel öneme sahiptir. Dalton Yasası ve mol kesri ilişkisi üzerinden bu değerlerin nasıl hesaplandığı, pratik çözüm adımları ve dikkat edilmesi gereken noktalarla birlikte ele alınmaktadır.
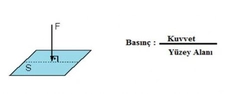
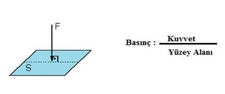
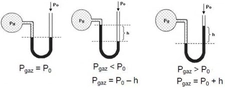
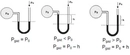
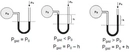
Kısmi Basınç Nedir?Bir gaz karışımında, her bir gaz bileşeninin tek başına kapladığı hacimde uygulayacağı basınca kısmi basınç denir. Dalton'un Kısmi Basınçlar Yasası'na göre, bir gaz karışımının toplam basıncı, karışımı oluşturan gazların kısmi basınçlarının toplamına eşittir. Yani: Ptoplam= P1+ P2+ P3+... şeklinde ifade edilir. Kısmi Basınç Hesaplama YöntemleriKısmi basınç hesaplamak için genellikle iki temel yöntem kullanılır: 1. Mol Kesri YöntemiBir gazın kısmi basıncı, toplam basınç ile o gazın mol kesrinin çarpımına eşittir: Pgaz= Xgaz× PtoplamBurada Xgaz, gazın mol kesridir ve şu şekilde hesaplanır: Xgaz= ngaz/ ntoplam 2. İdeal Gaz Denklemi YöntemiHer bir gaz bileşeni için ayrı ayrı ideal gaz denklemi uygulanabilir: Pgaz× V = ngaz× R × T Kısmi Basınç Problemlerini Çözme Adımları
Örnek Problem ve ÇözümüSoru:2 mol N2ve 3 mol O2gazlarının oluşturduğu karışımın toplam basıncı 5 atm'dir. Her bir gazın kısmi basıncını bulunuz.Çözüm:
Dikkat Edilmesi Gereken Noktalar
Pratik İpuçları
|