Osmotik basınç nasıl hesaplanır ve hangi formül kullanılır?
Yarı geçirgen bir zar aracılığıyla çözücü moleküllerin hareketini belirleyen osmotik basınç, hem laboratuvar ortamında hem de biyolojik sistemlerde kritik bir rol oynar. Bu kavram, çözünen madde konsantrasyonu ve sıcaklık gibi faktörlere bağlı olarak hesaplanabilirken, Van't Hoff faktörü iyonlaşma derecesini dikkate alarak formülün uygulanmasını sağlar.
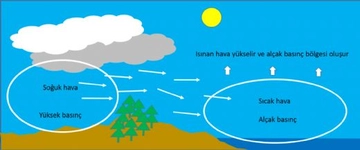
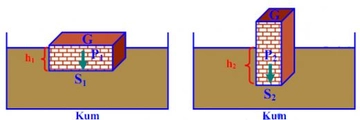
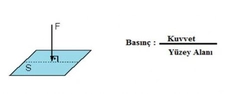
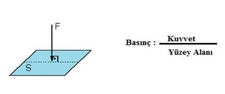
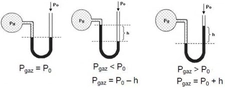
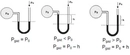
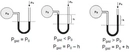
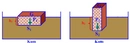
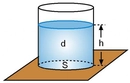
Osmotik Basınç Nedir?Osmotik basınç, bir çözeltinin yarı geçirgen bir zar üzerinden su çekme eğilimini ifade eden bir terimdir. Yarı geçirgen zar, çözücü moleküllerinin (genellikle su) geçişine izin verirken, çözünen moleküllerin geçişini engeller. Osmotik basınç, çözeltideki çözünen parçacıkların konsantrasyonuna bağlıdır ve ideal davranış gösteren seyreltik çözeltiler için hesaplanabilir. Osmotik Basınç Hesaplama FormülüOsmotik basınç (π), genellikle aşağıdaki formülle hesaplanır: Burada:
Van't Hoff Faktörü (i) Nedir?Van't Hoff faktörü, çözünen maddenin çözeltide kaç parçacığa ayrıştığını gösterir:
Hesaplama Örnekleri25°C'de 0.1 M glikoz çözeltisinin osmotik basıncı:
Aynı koşullarda 0.1 M NaCl çözeltisi:
Önemli Noktalar
Pratik Uygulamalar
|