Robert boyle, gazların basınç ve hacim ilişkisini incelemiş midir?
Gazların basınç ve hacim arasındaki ilişkisi, 17. yüzyılda Robert Boyle'un deneysel çalışmalarıyla bilim dünyasına kazandırıldı. Sabit sıcaklıkta gaz davranışlarını açıklayan bu temel prensip, modern termodinamiğin ve gaz yasalarının gelişiminde kritik bir rol oynamıştır.
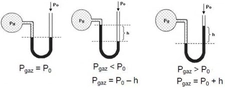
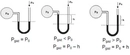
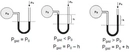
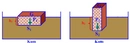
Evet, Robert Boyle gazların basınç ve hacim ilişkisini incelemiştir.Boyle Yasası (Boyle's Law) Nedir?Robert Boyle, 1662 yılında yaptığı deneyler sonucunda, sabit sıcaklıkta tutulan bir gazın basıncı ile hacmi arasında ters orantılı bir ilişki olduğunu keşfetti. Bu ilişki, Boyle Yasası olarak bilinir ve modern kimya ile fiziğin temel taşlarından biridir. Deneyin Özeti:Boyle, "U" şeklindeki bir cam tüp kullanarak deneyini gerçekleştirdi. Tüpün bir kolu kapalıydı ve içinde hapsedilmiş bir gaz vardı. Diğer kol ise açıktı ve civayla doluydu. Açık koldaki civa seviyesini değiştirerek kapalı koldaki gaza farklı basınçlar uyguladı. Her bir basınç değerinde, gazın hacmini ölçtü. Bulgular ve Matematiksel İfade:Yaptığı gözlemler sonucunda Boyle, sabit sıcaklıkta, bir gazın basıncı (P) ile hacminin (V) çarpımının sabit kaldığını buldu. Bu, aşağıdaki formülle ifade edilir: P₁V₁ = P₂V₂ Burada:
Başka bir deyişle, basınç arttıkça hacim azalır; basınç azaldıkça hacim artar. Önem ve Etkileri:Boyle'un bu çalışması:
Sonuç olarak, Robert Boyle gazların basınç ve hacim ilişkisini sadece incelemekle kalmamış, bu ilişkiyi niceliksel olarak tanımlayarak bilim tarihine damgasını vuran Boyle Yasası'nı formüle etmiştir. |