Osmotik basınç nedir ve nasıl hesaplanır?
Osmotik basınç, çözeltideki çözgen ve çözünmüş maddelerin etkileşimlerinden kaynaklanan bir kuvvettir. Bu basınç, yarı geçirgen bir membran aracılığıyla suyun hareketini dengeleyerek hücrelerin su dengesini sağlamada kritik rol oynar. Biyolojik sistemlerdeki önemi, çeşitli uygulamalarda da kendini gösterir.
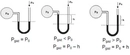
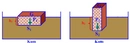
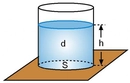
Osmotik Basınç Nedir?Osmotik basınç, bir çözelti içindeki çözücü ve çözgen molekülleri arasındaki etkileşimlerin bir sonucudur. Bu basınç, bir çözelti ile saf su veya başka bir çözelti arasındaki yarı geçirgen bir membran üzerinden çözgenin geçişini dengeleyen kuvvet olarak tanımlanır. Osmotik basınç, çözelti içindeki çözünmüş madde miktarına bağlı olarak değişir ve genellikle yüksek çözünürlüklü çözeltilerde daha yüksektir. Bu basınç, hücrelerin su dengesinin korunmasında kritik bir rol oynar ve biyolojik sistemlerde önemli bir işlevi vardır. Osmotik Basıncın ÖnemiOsmotik basınç, birçok biyolojik ve kimyasal süreçte önemli bir rol oynar. Örneğin, bitkilerde suyun köklerden yapraklara taşınmasında, hayvan hücrelerinde ve insan vücudunun sıvı dengesinin sağlanmasında kritik bir faktördür. Ayrıca, tıbbi uygulamalarda, özellikle intravenöz sıvı tedavisinde, osmotik basıncın anlaşılması hayati önem taşır. Osmotik Basınç Nasıl Hesaplanır? Osmotik basıncı hesaplamak için genellikle Van 't Hoff denklemi kullanılır. Bu denklem aşağıdaki gibi ifade edilir: Osmotik Basıncın Uygulamaları Osmotik basıncın pratikte birçok uygulaması bulunmaktadır:
Sonuç Osmotik basınç, çözelti içindeki çözünmüş maddelerin etkisiyle oluşan bir basınçtır ve birçok biyolojik ve kimyasal süreç için kritik bir öneme sahiptir. Van 't Hoff denklemi kullanılarak hesaplanan osmotik basınç, çeşitli bilim ve mühendislik alanlarında önemli uygulamalara sahiptir. Osmotik basıncın anlaşılması, hem temel bilimler hem de uygulamalı alanlarda önemli bilgiler sunar. Ek Bilgiler - Osmotik basınç, deniz suyu ve tatlı su arasındaki su hareketini etkileyen faktörlerden biridir.- Yüksek osmotik basınca sahip çözeltiler, suyun daha düşük osmotik basınca sahip çözeltilere doğru hareket etmesine neden olur, bu da hücrelerin şişmesine veya büzülmesine yol açabilir.- Osmotik basıncı etkileyen diğer faktörler arasında sıcaklık, çözücüler ve çözünmüş maddelerin türleri de bulunmaktadır. |