
Kısmi basınç formülü nedir ve nasıl uygulanır?
Kısmi basınç, bir gaz karışımındaki her gazın, toplam basıncı etkileyen diğer gazların varlığından bağımsız olarak oluşturduğu basınçtır. Dalton'un Kısmi Basınçlar Yasası'na göre, toplam basınç, her gazın kısmi basınçlarının toplamına eşittir. Bu kavram, gazların davranışını anlamada ve kimyasal süreçlerin analizinde kritik bir öneme sahiptir.
Kısmi Basınç Formülü Nedir?Kısmi basınç, bir gaz karışımındaki her bir gazın, toplam basıncı etkileyen diğer gazların varlığından bağımsız olarak oluşturduğu basınçtır. Kısmi basınç, Dalton'un Kısmi Basınçlar Yasası'na dayanır; bu yasaya göre, bir gaz karışımındaki toplam basınç, her bir gazın kısmi basınçlarının toplamına eşittir. Matematiksel olarak ifade edersek: P_total = P1 + P2 + P3 +... + Pn Burada, P_total toplam basıncı, P1, P2, P3,... Pn ise her bir gazın kısmi basıncını temsil eder. Kısmi basınç, gazların mol sayısına ve toplam gaz karışımındaki oranına bağlıdır. Kısmi Basınç Formülünün UygulanmasıKısmi basınç formülünün uygulanması, çeşitli alanlarda önemli sonuçlar elde edilmesine olanak tanır. Bu alanlar arasında kimya, fizik ve mühendislik gibi alanlar bulunmaktadır. Uygulama süreci genel olarak aşağıdaki adımlar izlenerek gerçekleştirilir:
Örnek UygulamaBir gaz karışımında, 3 mol azot (N2) ve 2 mol oksijen (O2) bulunmaktadır. Bu karışımın toplam basıncı 5 atm olarak ölçülmüştür. Kısmi basınçları hesaplamak için öncelikle toplam mol sayısını bulmalıyız:- n_total = n_N2 + n_O2 = 3 mol + 2 mol = 5 molDaha sonra, her gazın kısmi basıncını hesaplayalım:- P_N2 = (n_N2 / n_total) P_total = (3 mol / 5 mol) 5 atm = 3 atm- P_O2 = (n_O2 / n_total) P_total = (2 mol / 5 mol) 5 atm = 2 atmBu durumda, azotun kısmi basıncı 3 atm, oksijenin kısmi basıncı ise 2 atm olarak bulunur. SonuçKısmi basınç formülü, gaz karışımlarının analizinde ve çeşitli kimyasal işlemlerin anlaşılmasında önemli bir araçtır. Gazların davranışlarını anlamak, endüstriyel süreçlerde ve laboratuvar çalışmalarında büyük kolaylık sağlar. Kısmi basınçların doğru bir şekilde hesaplanması, gazların karışım oranlarını ve etkileşimlerini anlamak için kritik öneme sahiptir. Ekstra Bilgiler |















Kısmi basınç formülü hakkında daha fazla bilgi edinmek istiyorum. Özellikle, gaz karışımlarında her bir gazın kısmi basıncını hesaplamak için gereken adımların detaylarını anlamak istiyorum. Örneğin, toplam basıncı ölçme ve gazların mol sayısını belirlemede karşılaştığınız zorluklar nelerdi? Bu süreçte hangi yöntemleri kullandınız? Kısmi basınçların hesaplanması sırasında dikkat edilmesi gereken önemli noktalar var mı?
Kısmi Basınç Nedir?
Kısmi basınç, bir gazın karışımdaki toplam basınca katkıda bulunan basıncını ifade eder. Dalton'un Kısmi Basınçlar Yasası'na göre, bir gaz karışımındaki her bir gazın kısmi basıncı, o gazın toplam karışım içindeki mol fraksiyonuna eşittir.
Kısmi Basıncı Hesaplama Adımları
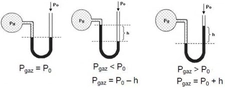
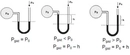
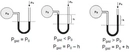
1. Toplam Basıncı Ölçme: İlk olarak, karışımın toplam basıncını ölçmelisiniz. Bu, genellikle bir manometre ile yapılır.
2. Gazların Mol Sayısını Belirleme: Karışımdaki her bir gazın mol sayısını belirlemek için, gazların hacimlerini, sıcaklıklarını ve basınçlarını kullanarak ideal gaz yasası (PV=nRT) ile hesaplama yapabilirsiniz.
3. Mol Fraksiyonunu Hesaplama: Her bir gazın mol sayısını toplam mol sayısına bölerek mol fraksiyonunu bulmalısınız. Örneğin, bir gazın mol sayısı 'n1' ve toplam mol sayısı 'n_total' ise, mol fraksiyonu 'y1 = n1/n_total' olarak hesaplanır.
4. Kısmi Basıncı Hesaplama: Kısmi basıncı bulmak için, toplam basıncı mol fraksiyonuyla çarpın. Yani, p1 = P_total y1.
Zorluklar ve Yöntemler
Toplam basıncı ölçmek genellikle daha kolaydır; ancak, gazların mol sayısını belirlerken bazı zorluklar ortaya çıkabilir. Gazların sıcaklık ve basınç koşulları değiştiğinde, ideal gaz yasası geçerliliğini kaybedebilir. Bu durumda, gerçek gaz davranışını göz önünde bulundurarak Van der Waals gibi düzeltme faktörleri kullanmak gerekebilir.
Dikkat Edilmesi Gereken Noktalar
1. Sıcaklık ve Basınç Değişimleri: Gazların sıcaklık ve basınç değişimlerinin kısmi basınç hesaplamalarına etkisini dikkate almak önemlidir.
2. Gazların Karşılıklı Etkileşimleri: Gaz karışımlarında, gazlar arasındaki etkileşimlerin kısmi basınçlarda değişiklik yaratabileceğini unutmamak gerekir.
3. Hesaplama Hataları: Ölçüm aletlerinin doğruluğu ve hesaplama sırasında yapılan hatalar, sonuçları etkileyebilir. Bu nedenle, her adımda dikkatli olunmalıdır.
Bu adımları izleyerek ve dikkatli hesaplamalar yaparak, gaz karışımlarındaki kısmi basınçları doğru bir şekilde hesaplayabilirsiniz.