
Osmotik Basınç Nasıl Hesaplanır?
Osmotik basınç, bir çözeltinin su ile etkileşimi sırasında ortaya çıkan basınçtır ve biyolojik sistemlerde sıvı dengesini sağlamada kritik bir rol oynar. Hesaplama formülüyle belirlenen bu kavram, çeşitli bilimsel ve endüstriyel uygulamalarda önem taşır.
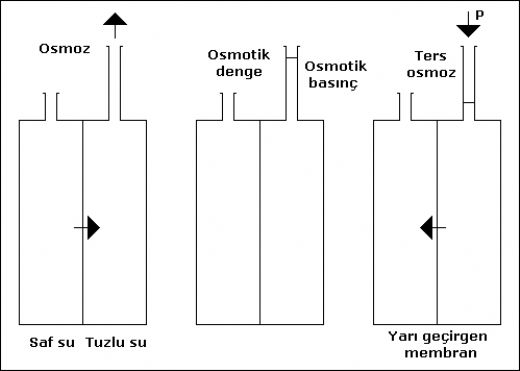
Osmotik Basınç Nedir?Osmotik basınç, bir çözelti ile saf su arasında, çözelti tarafından uygulanan bir basınçtır. Bu basınç, çözücünün (genellikle su) yarı geçirgen bir zar aracılığıyla çözeltinin yoğunluğuna bağlı olarak hareket etme eğiliminden kaynaklanır. Osmotik basınç, özellikle biyolojik sistemlerde sıvı dengesinin sağlanması açısından kritik öneme sahiptir. Bu durum, hücrelerin su alıp verme süreçlerini etkileyerek, hücrelerin osmotik dengesini ve dolayısıyla yaşam fonksiyonlarını etkileyebilir. Osmotik Basınç Hesaplama Formülü Osmotik basıncı hesaplamak için genellikle Van 't Hoff denklemi kullanılır. Bu denkleme göre, osmotik basınç (π) aşağıdaki formülle hesaplanır:\[ \pi = i \cdot C \cdot R \cdot T \]Burada;
Bu formül, çözeltinin özelliklerine ve mevcut koşullara göre değişiklik gösterebilir. Örneğin, çözeltinin sıcaklığı arttıkça osmotik basınç da artar. Osmotik Basınç ve İyonlaşma Faktörü Osmotik basınç hesaplamasında önemli bir parametre olan Van 't Hoff faktörü (i), çözeltinin iyonlaşma derecesini ifade eder. İyonlaşma, bir molekülün çözünme sırasında iyonlara ayrılması anlamına gelir. Örneğin;
Bu faktör, çözeltinin osmotik basıncını doğrudan etkiler ve doğru bir hesaplama için dikkate alınmalıdır. Osmotik Basınç Uygulamaları Osmotik basınç, pek çok alanda önemli uygulamalara sahiptir;
Osmotik basınç, aynı zamanda su arıtma teknolojilerinde de önemli bir rol oynamaktadır. Ters osmoz, suyun tuzdan arındırılması için kullanılan bir yöntemdir ve bu işlemde osmotik basınç temel bir faktördür. Sonuç Osmotik basınç, hem fiziksel hem de biyolojik süreçlerin anlaşılmasında kritik bir kavramdır. Çözeltinin molar konsantrasyonu, sıcaklık ve iyonlaşma derecesi gibi faktörler, osmotik basıncın hesaplanmasında önemli rol oynamaktadır. Bu kavram, birçok bilim dalında ve endüstriyel uygulamalarda geniş bir yelpazede kullanılmaktadır. Osmotik basıncın doğru bir şekilde hesaplanması ve anlaşılması, hem temel bilimlerde hem de uygulamalı alanlarda büyük önem taşımaktadır. |















Osmotik basınçla ilgili bir proje üzerinde çalışıyorum ve denklemi kullanarak hesaplamalar yapmam gerekiyor. Van't Hoff faktörünün özellikle hangi durumlarda önemli olduğunu daha ayrıntılı açıklayabilir misiniz? Ayrıca, seyreltilmiş çözeltiler dışında osmotik basıncı hesaplarken nelere dikkat etmeliyim?
Oğur, merhaba. Van't Hoff faktörü (i), özellikle elektrolit çözeltilerinde önemlidir. Bu faktör, bir çözeltinin osmotik basıncını hesaplarken, çözeltideki iyon sayısını dikkate alarak gerçek davranışını daha doğru bir şekilde yansıtır. Örneğin, NaCl gibi bir tuz suda çözüldüğünde, Na+ ve Cl- olarak iki iyon oluşturur ve bu da osmotik basıncı arttırır.
Seyreltilmiş çözeltiler dışında osmotik basıncı hesaplarken şunlara dikkat etmelisiniz:
1. Gerçek çözeltilerin davranışı: Konsantrasyon arttıkça, çözeltinin davranışı ideal olmaktan sapar.
2. Sıcaklık: Sıcaklık artışı, genellikle osmotik basıncı da arttırır.
3. Kolligatif özellikler: Çözeltinin diğer kolligatif özellikleri (kaynama noktasi yükselmesi, donma noktası düşmesi) de osmotik basıncı etkileyebilir.
4. Çözeltinin bileşimi: Çözeltideki çeşitli bileşenlerin etkileşimleri de osmotik basıncı etkileyebilir.
Bu faktörleri dikkate alarak hesaplamalarınızı yaparsanız, daha doğru ve güvenilir sonuçlar elde edebilirsiniz. Kolay gelsin!